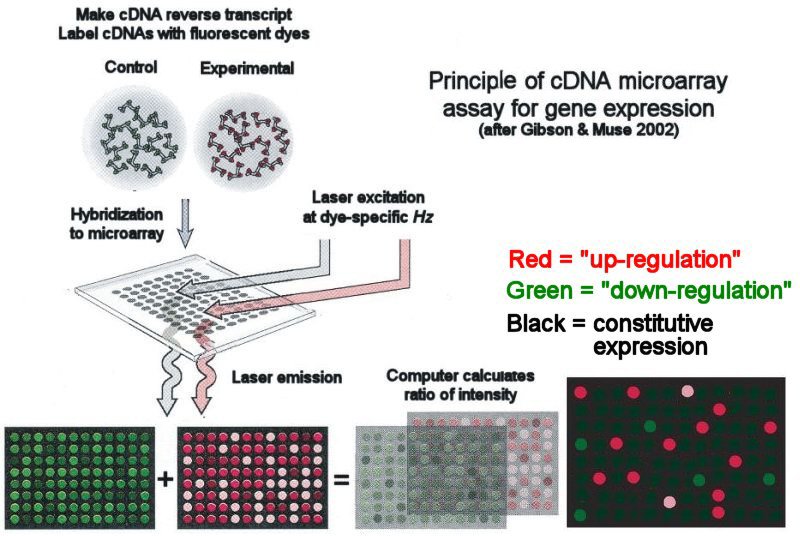
ADN RECOMBINANTE EN LA NATURALEZA
La gran abundancia de genes de origen bacteriano en el genoma nuclear de P. purpureum ha sido de gran interés por ello han secuenciado ese genoma demostrando un sistema de transformación genética que parece exhibir una tasa relativamente alta de recombinación homóloga. El mantenimiento del plásmido en P. purpureum. depende de los orígenes bacterianos de la replicación y, por lo tanto, representa un caso interesante de intercambio de ADN y compatibilidad genética entre dos dominios diferentes de la vida (bacterias y eucariotas). Por lo tanto, proponemos que la presencia frecuente de plásmidos en las algas rojas podría explicarse por la compatibilidad de los sistemas de replicación de plásmidos en bacterias con la maquinaria de replicación de ADN que opera en el núcleo de algas rojas.
Las
bacterias sufren varias tipos de recombinación que hace posible la
transferencia de genes entre especies no afines. Un proceso conocido como la
transformación permite que las bacterias capturen DNA libre del ambiente. También puede haber transformación cuando las bacterias capturan diminutas moléculas
circulares de ADN llamados plásmidos.
La gran abundancia de genes de origen bacteriano en el genoma nuclear de P. purpureum ha sido de gran interés por ello han secuenciado ese genoma demostrando un sistema de transformación genética que parece exhibir una tasa relativamente alta de recombinación homóloga. El mantenimiento del plásmido en P. purpureum. depende de los orígenes bacterianos de la replicación y, por lo tanto, representa un caso interesante de intercambio de ADN y compatibilidad genética entre dos dominios diferentes de la vida (bacterias y eucariotas). Por lo tanto, proponemos que la presencia frecuente de plásmidos en las algas rojas podría explicarse por la compatibilidad de los sistemas de replicación de plásmidos en bacterias con la maquinaria de replicación de ADN que opera en el núcleo de algas rojas.
ADN RECOMBINANTE ARTIFICIAL

Una
nueva vacuna contra la influenza A se realizó mediante la fusión genética de
los aminoácidos 2–16 de M2e (proteína matriz 2) del virus al extremo N de la proteína pVIII de la
cubierta principal para generar fagos híbridos que contienen capsómeros. Los fagos
f88 − M2e2-16 recombinantes resultantes que forman una estructura helicoidal
alrededor del ADN genómico circular monocatenario no matan a su huésped, sino
que se comportan como una infección persistente que frena el crecimiento
bacteriano, con nuevos fagos que brotan continuamente de la E. coli. La
inmunización con f88M2e2-16 indujo niveles de anticuerpos protectores mejorados
dramáticamente después de la segunda y tercera inyección y confirió una
protección completa.
REFERENCIAS BIBLIOGRÁFICAS
1. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6110788/
2. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4431709/
3.https://espanol.cdc.gov/enes/flu/protect/vaccine/qa_flublok-vaccine.htm
4. https://www.ncbi.nlm.nih.gov/books/NBK21881/